INTRODUCTION
La migraine est vue aujourd’hui comme une maladie génétique et les crises s’expliquent comme étant une mauvaise adaptation du cerveau au changement. Un cerveau génétiquement déterminé pour être migraineux est un cerveau dont l’hypothalamus – dont on sait qu’il est le générateur des crises - est très sensible aux divers changements (sommeil, repas, émotions, rythme de vie, activités diverses…), et notamment aux variations hormonales. Or les grandes fluctuations hormonales, dans un sens ou un autre, sont présentes tout au long de la vie de la femme, à l’occasion – entre autres - des règles ou de la ménopause.
Le mécanisme des crises migraineuses est complexe mais les hormones sexuelles féminines semblent intervenir, en particulier les œstrogènes. Globalement, les crises de migraine chez les femmes sont calquées sur les fluctuations hormonales : elles débutent souvent à la puberté, sont plus fréquentes lors des règles, et ont tendance à diminuer après la ménopause et avec la grossesse (en dehors des migraines avec aura), les hormones sexuelles étant sécrétées de manière homogène pendant cette période. En dehors de la grossesse, un traitement contraceptif ou hormonal substitutif de la ménopause peut aussi intervenir, en atténuant les fluctuations hormonales physiologiques.
En 2022, la Société française d’étude des migraines et céphalées (SFEMC) a publié de nouvelles recommandations spécifiques à la prise en charge de la migraine chez la femme [1].
ÉPIDÉMIOLOGIE
Deux migraineux sur trois sont des femmes. Environ 5 millions de Françaises sont migraineuses. Il existe un lien très clair entre migraine et hormones féminines, essentiellement les œstrogènes. Cela explique probablement la plus grande fréquence de la migraine chez les femmes comparé aux hommes. Une hypothèse renforcée par le fait qu’avant la puberté, filles et garçons sont autant migraineux les uns que les autres. À la puberté, le ratio bascule et les femmes deviennent majoritaires.
ÉLÉMENTS PHYSIOPATHOLOGIQUES DES CÉPHALÉES MIGRAINEUSES
La physiopathologie des céphalées migraineuses fait intervenir le système trigémino-vasculaire. Celui-ci libère des médiateurs algiques lors de la crise migraineuse, comme le CGRP-peptide (calcitonin gene-related peptide ou peptide relié au gène de la calcitonine). La relation entre les variations de CGRP et les hormones sexuelles chez les femmes migraineuses est peu connue. Une étude cas-témoin parue en mai 2023 [2] conclut, tout en soulignant les nombreux biais potentiels de l’analyse, que la chute des taux d’œstrogènes en début de règles semble coïncider avec une élévation de la CGRP, rendant compte des crises de migraine survenant au début des règles ou au cours de celles-ci. Les fluctuations hormonales modifieraient ainsi les concentrations en CGRP chez les migraineuses. Ces données restent à approfondir.
LES MIGRAINES MENSTRUELLES
Au cours des migraines qui surviennent pendant les règles (cataméniales), c’est la chute du taux d’œstrogènes qui est à l’origine de la crise migraineuse. La Classification internationale des céphalées (ICHD-3) [3] distingue depuis 2018 deux types de crises en relation avec les règles.
➔ La migraine menstruelle pure est diagnostiquée lorsque les crises surviennent exclusivement au moment des règles, c’est-à-dire le 1er jour des règles (+/- 2 jours), sur au moins deux cycles menstruels sur trois, et à aucun autre moment du cycle. De nombreuses femmes surestiment l’association exclusive entre les crises de migraine et les menstruations, et seules 8 % d’entre elles souffrent de migraine menstruelle pure [4].
➔ La majorité des femmes souffrent plutôt de « migraine liée aux menstruations », avec des crises survenant pendant, mais aussi en dehors du cycle : les crises se manifestent le 1er jour des règles (+/- 2 jours), sur au moins deux cycles sur trois, ainsi qu’à d’autres moments du cycle.
Les triptans, les AINS (naproxène), le paracétamol et l’association aspirine-caféine sont des traitements de crise efficaces de la migraine menstruelle (les deux formes).
Toutefois, les crises menstruelles, le plus souvent sans aura, sont plus longues que les crises communes, plus invalidantes, plus souvent associées à des nausées et répondent moins bien au traitement des crises, d’où l’association quasi-systématique d’un triptan et d’un anti-inflammatoire. Trois triptans se sont avérés efficaces dans ce cas précis : frovatriptan 2,5 mg et naratriptan 2,5 mg deux fois par jour, zolmitriptan 2,5 mg trois fois par jour.
Les femmes souffrant de migraines fréquentes incluant des crises menstruelles s’exprimant sur une modalité élevée peuvent bénéficier de médicaments prophylactiques ou traitement de fond. On a longtemps proposé à ces femmes des traitements séquentiels, c’est-à-dire la prescription de petites doses d’œstrogènes ou d’anti-inflammatoire (naproxène) avant la survenue des règles. C’est en réalité peu ou pas efficace car, pour que cela fonctionne, il faut une régularité parfaite du cycle menstruel ainsi que des crises migraineuses très ponctuelles au cours des règles, ce qui reste exceptionnel.
Chez les femmes éligibles, la contraception hormonale peut être utilisée dans le but de prévenir la migraine menstruelle (prise continue de la contraception, ou intervalle sans hormone plus court).
LA CONTRACEPTION
En termes de contraception, dans les migraines sans aura (80 % des migraineuses), et en l’absence de risque artériel (âge > 35 ans, tabagisme chez les plus de 35 ans, hypertension artérielle, dyslipidémie, diabète, obésité, antécédents familiaux d’AVC ou d'infarctus du myocarde), la prescription de pilules, notamment œstroprogestatives, est possible. Leur impact sur la migraine peut être positif, négatif ou neutre.
En revanche, dans les migraines avec aura, qui confèrent un surrisque artériel, la contraception œstroprogestative est contre-indiquée. Les pilules progestatives pures, le stérilet au cuivre ou le dispositif intra-utérin (DIU) au lévonorgestrel sont des alternatives envisageables ; la contraception progestative n’étant pas associée à un risque accru d’accident vasculaire cérébral ischémique.
Aucune étude n’a été publiée concernant l’impact du dispositif intra-utérin au lévonorgestrel sur la migraine, son évolution ou les crises elles-mêmes.
LORS DE LA GROSSESSE
La migraine sans aura s’améliore généralement, voire disparaît, pendant la grossesse, surtout après le premier trimestre [5]. Chez deux tiers des femmes, la grossesse constitue une période de répit vis-à-vis des migraines sans aura (période qualifiée de « lune de miel »), le plus souvent pendant les deux derniers trimestres, du fait d’une sécrétion œstrogénique homogène. Il est estimé, selon les études, que seules 20 % des femmes migraineuses auront au moins une crise pendant la grossesse [6].
C’est l’inverse chez les femmes migraineuses avec aura qui sont enceintes, chez lesquelles les crises ont tendance à persister voire à s’aggraver.
De manière générale, les femmes migraineuses doivent être suivies d’encore plus près du fait d’un risque accru de prééclampsie et de petit poids de naissance.
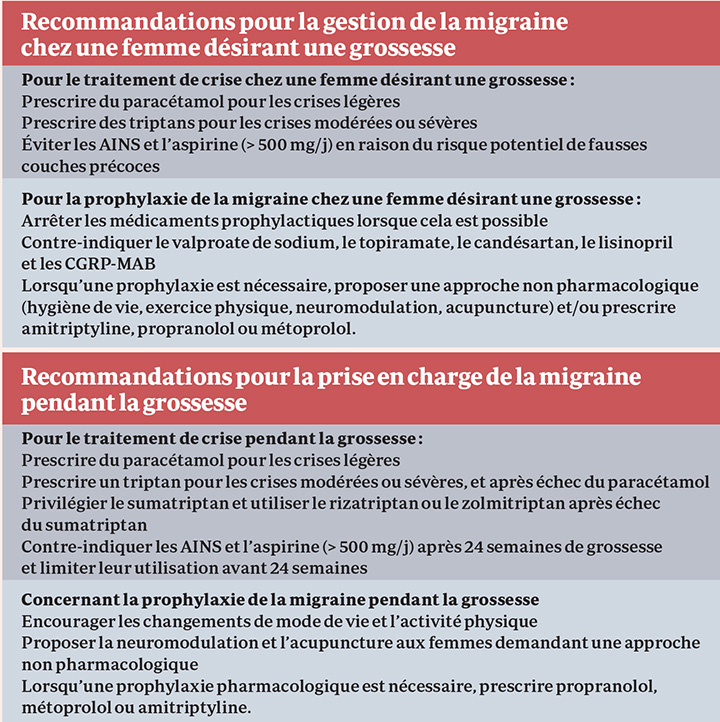
➔ En traitement de crise
Concernant les crises migraineuses, on a longtemps accordé à la femme enceinte le seul paracétamol. En 2023, le recul est suffisant pour conseiller d’autres thérapeutiques, comme les triptans (commercialisés depuis 30 ans), dont le sumatriptan en 1re ligne. Le Centre de référence français des agents tératogènes (CRAT) recommande de privilégier le sumatriptan après échec du paracétamol, puis le zolmitriptan ou le rizatriptan après échec du sumatriptan [7]. Quant aux anti-inflammatoires (AINS), ils sont contre-indiqués à partir du de 24 semaines de grossesse, en raison du risque de fermeture prématurée du canal artériel. Certaines études ont aussi suggéré d’éviter les AINS au cours du premier trimestre de grossesse, même si la question de savoir s’ils augmentent le risque de fausse couche reste posée mais non résolue [8]. Un travail récent fondé sur une large base de données a montré que les risques d’avortement spontané et de malformations congénitales majeures ne différaient pas entre les femmes exposées et non exposées à l’ibuprofène (niveau de preuve moyen) [9]. Le CRAT recommande d’éviter les AINS de manière chronique avant 24 SA et autorise une utilisation ponctuelle. Par prudence, les neurologues à l’origine des recommandations conseillent de les éviter le plus possible, même en début de grossesse.
➔ En prophylaxie anti-migraineuse
Outre le traitement de crise, il n’y a pas d’alerte avec certains traitements de fond prescrits chez la femme enceinte, dont les bétabloquants (recommandés en première ligne) comme le métoprolol ou le propranolol. Les bétabloquants ne sont pas associés à un risque accru de malformations, et ceci dispose d’un niveau de preuve élevé [10]. Pour sa part, l’amitriptyline peut être utilisée du fait de données nombreuses et rassurantes pendant la grossesse [11].
Selon le CRAT, la venlafaxine peut également être utilisée pendant la grossesse chez les femmes présentant une dépression nécessitant un traitement pharmacologique. Elle peut donc être utilisée chez les femmes présentant une dépression et une migraine associée pendant la grossesse.
En revanche, dès le désir d’enfant et pendant la grossesse, certains médicaments sont contre-indiqués. Il s’agit de l’acide valproïque et du topiramate (risque de malformations et risque autistique), du candésartan et du lisinopril en raison de leur toxicité rénale fœtale, ainsi que tous les dérivés ergotés. Faute de recul, les anticorps anti-CGRP, comme l’érénumab, restent contre-indiqués par précaution. À noter, les quelques retours d’études conduites en vraie vie sont rassurants concernant ces nouvelles thérapeutiques anti-migraineuses (disponibles mais encore non remboursées en France).
À LA MÉNOPAUSE
Si la migraine a tendance à s’améliorer à la ménopause, la périménopause est souvent associée à̀ une hausse de la fréquence des crises [12]. La présence d’une migraine avec aura ne contre-indique pas l’utilisation d’œstrogènes transdermiques en tant que traitement hormonal de la ménopause (THM). Attitude dictée par le bon sens, il est déconseillé d’instaurer simultanément un THM et un traitement de fond car il ne sera alors pas possible d’évaluer séparément l’impact de l’un et de l’autre sur les crises de migraine. Procéder étape par étape est préférable, assorti de réévaluations régulières.
EN RÉSUMÉ
- Dans les migraines avec aura, du fait d’un surrisque artériel, la contraception œstroprogestative est contre-indiquée.
- Les crises menstruelles sont le plus souvent sans aura. Elles sont plus durables que les crises communes, plus invalidantes, d’où l’association quasi-systématique d’un triptan et d’un anti-inflammatoire.
- La prescription de paracétamol mais aussi de certains triptans est possible chez la femme enceinte en traitement de crise migraineuse, dont le sumatriptan en 1re ligne. Une prophylaxie anti-migraineuse est possible, avec une grande vigilance vis-à-vis des risques liés aux différentes molécules.
- En cas de migraine invalidante au cours de la grossesse, la patiente doit être suivie conjointement par un neurologue et un gynécologue.
- Les migraines sans aura comme celles avec aura ne constituent pas des contre-indications à l’utilisation d’œstrogènes transdermiques en tant que traitement hormonal de la ménopause.
Hélène Joubert, rédactrice, avec le Pr Anne Donnet (CHU de Marseille), coauteure des « Recommandations de la Société française d’étude des migraines et céphalées (SFEMC) sur les situations spécifiques chez les femmes migraineuses » (1).
BIBLIOGRAPHIE
1. Ducros A, Donnet A, Demarquay G. Recommandations pour le diagnostic et la prise en charge de la migraine chez l'adulte : situations spécifiques chez les femmes migraineuses. Presse Med Form 2022; 3: 421–426 (disponibles en ligne en mars 2023).
2. Marcus R. Study Provides New Insight Into Female Sex Hormones and Migraines. Jama. 2023 May 2;329(17):1439-1440. doi: 10.1001/jama.2023.5536
3. Headache Classification Committee of the International Headache Society (IHS). The International Classification of Headache Dis- orders, 3rd edition. Cephalalgia Int J Headache 2018;38:1-211. https://doi.org/10.1177/ 0333102417738202.
4. Burch R. Epidemiology and treatment of menstrual migraine and migraine during pregnancy and lactation: a narrative review. Headache 2020;60:200–16.
5. Kvisvik EV, Stovner LJ, Helde G, Bovim G, Linde M. Headache and migraine during pregnancy and puerperium: the MIGRA-study. J Headache Pain 2011;12:443–51.
6. Tanos V, Raad EA, Berry KE, Toney ZA. Review of migraine incidence and management in obstetrics and gynaecology. Eur J Obstet Gynecol Reprod Biol 2019;240:248–55.
7. Centre de référence des agents tératogènes, 2020. https://www.lecrat.fr. n.d.
8. Li DK, Ferber JR, Odouli R, Quesenberry C. Use of nonsteroidal antiinflammatory drugs during pregnancy and the risk of miscarriage. Am J Obstet Gynecol 2018;219:275.e1–.e8.
9. Dathe K, Fietz AK, Pritchard LW, Padberg S, Hultzsch S, Meixner K, et al. No evidence of adverse pregnancy outcome after exposure to ibuprofen in the first trimester - Evaluation of the national Embryotox cohort. Reprod Toxicol Elmsford N 2018;79:32–8.
10. Wu Y, Yao JW, Xu LJ, Chen M, Wan L. Risk of congenital malformations in offspring of women using b-blockers during early pregnancy : An updated meta-analysis of observational studies. Br J Clin Pharmacol 2021;87:806–15.
11. Gérard A, Zhao JP, Sheehy O. Antidepressant use during pregnancy and the risk of major congenital malformations in a cohort of depressed pregnant women: an updated analysis of the Quebec Pregnancy Cohort. BMJ Open 2017;7:e013372.
12. MacGregor EA. Migraine, menopause and hormone replacement therapy. Post Reprod Health 2018;24:11–8.
Liens d'intérêts : Les auteurs déclarent n'avoir aucun lien d'intérêts relatif au contenu de cet article


Mise au point
Le prurit
Mise au point
Les infiltrations en médecine générale
Mise au point
Diagnostic de la maladie d’Alzheimer en 2025
Étude & pratique
Apnées du sommeil : quel impact de la ventilation sur la mortalité ?